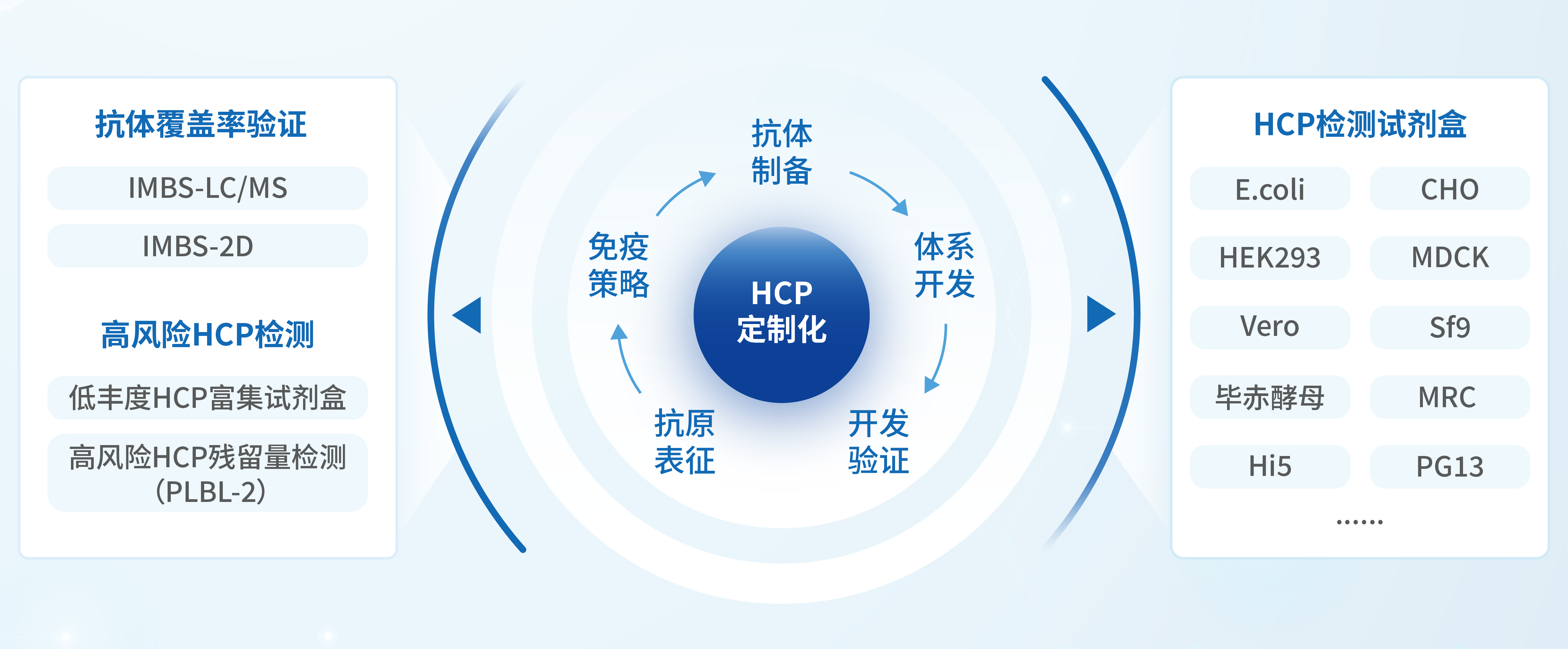
产品中心
在生物制药CMC(化学、制造与控制)领域,宿主细胞蛋白(Host Cell Proteins, HCP)的残留检测始终是工艺验证和放行检测的核心环节。作为金标准的ELISA方法,尽管在灵敏度和通量上具有优势,但在实际操作与样品检测过程中,分析人员常面临特异性不足、稀释非线性、回收率异常等技术瓶颈。
这些问题不仅影响数据可靠性,更可能导致工艺决策偏差。本文将深入剖析这三大痛点的成因,并提供经过验证的实操解决方案。
01 特异性缺陷:当抗体"认错"靶标
特异性是HCP ELISA的根基,但可能会出现检测用抗体与产品主蛋白或制剂成分发生非特异性结合,导致假阳性;或者是抗体覆盖率不足,特别是对低分子量或酸性HCP的识别能力弱,造成假阴性的情况发生。
• 系统性解决方案 1: 抗体特异性验证
在试剂盒早期选用时,应当采用合适的方法对抗体特异性进行验证,以评估适用性情况。如果是采用定制化服务的,应当在开发早期对血清或抗体来源进行表征与筛选,以降低开发失败的风险。
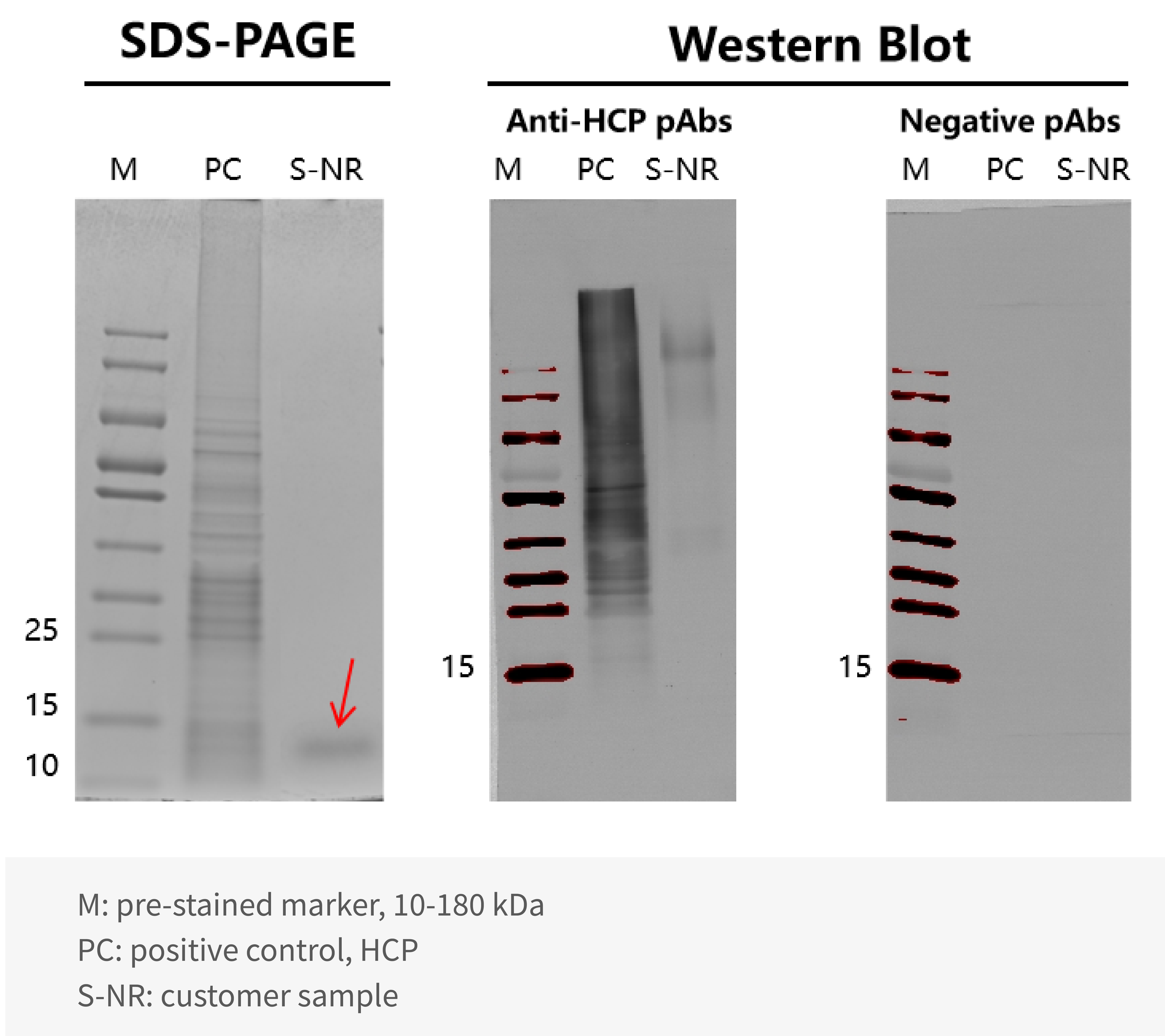
湖州申科基于客户样品,在试剂盒选型过程中提供抗体特异性分析服务,为方法开发奠定可靠基础。
• 系统性解决方案 2:抗体覆盖率验证
采用凝胶电泳/免疫印迹(2D-PAGE/WB)或者质谱鉴定(LC-MS/MS)等相关手段进行抗体覆盖率评估。对于文献已报道或者工艺特异性相关的高风险蛋白,建议采用正交方法补充检测。
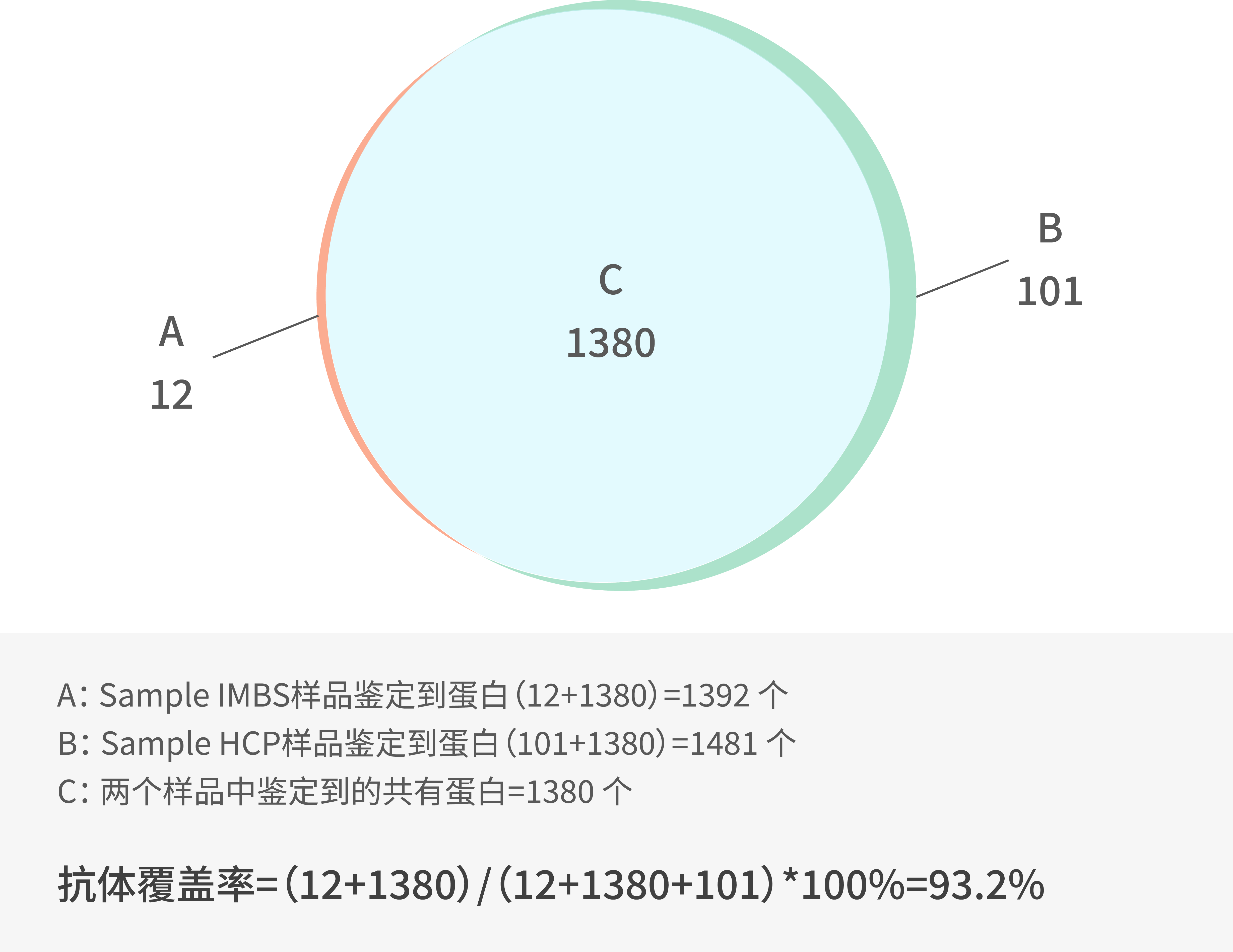
湖州申科采用IMBS®-MS专利技术,提供基于客户样品的抗体覆盖率分析服务,确保试剂盒选型精准高效。
二、稀释非线性:Hook效应的陷阱
校准曲线线性良好,但待测样品系列稀释后浓度回算值出现系统性偏离(一般应满足80%-120%),这通常由于Hook效应(极高浓度HCP导致抗原过量,阻碍三明治复合物形成,造成假性低值)造成的。在实际情况中,由于HCP的分布不均,Hook效应往往不是所有蛋白,而是其中的个别蛋白引起的。
• 实操解决方案 1: 稀释线性验证
根据法规,确定样品最小稀释倍数(MRD),即在样品空白基质中加入高浓度HCP校准品,进行系列梯度稀释,选择满足要求的最低MRD。确定MRD后,所有样品必须至少以MRD进行预稀释,以消除基质效应。
DF | BackCalc. Conc. (ng/mL) | DF-corrected Conc. (ng/mL) | MRD (%) |
25 | 65.1 | 1627.5 | / |
50 | 39.3 | 1965.9 | 121% |
100 | 24.3 | 2430.2 | 124% |
200 | 16.6 | 3313.9 | 136% |
400 | 9.4 | 3744.3 | 113% |
800 | 5.1 | 4054.0 | 108% |
1600 | 2.6 | 4161.2 | 103% |
3200 | 1.3 | 4295.1 | 103% |
湖州申科基于客户实际基质的MRD验证实例。在样品基质中添加HCP校准品蛋白,根据预期浓度进行梯度稀释。结果显示,在满足稀释线性的要求下,实际样品在检测时,需要至少稀释400倍才可满足方法学适用要求。此结果可供后续样品检测提供参考。
• 实操解决方案 2:正交方案验证
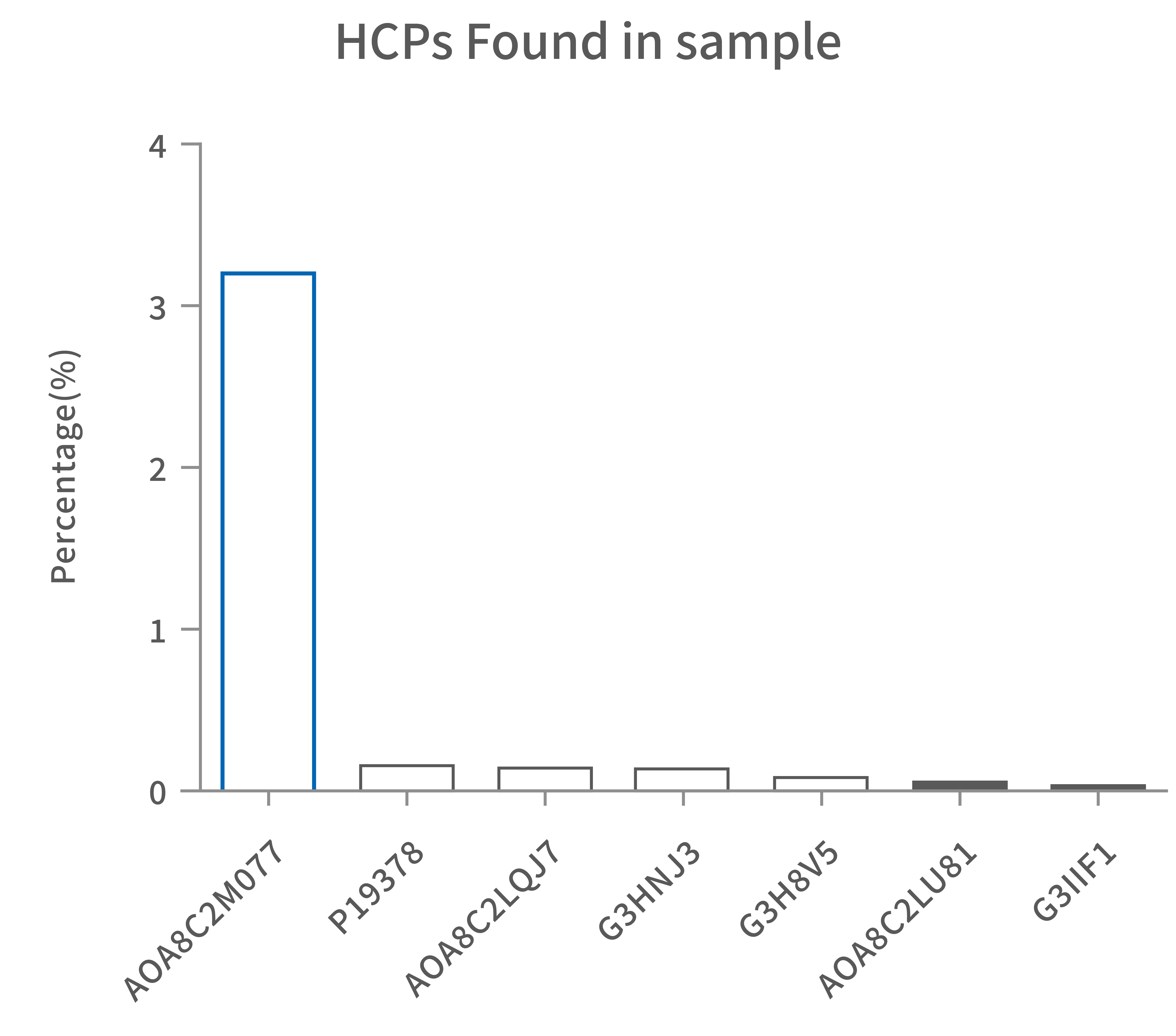
在样品适用性阶段,建议采用质谱等手段确认实际样品HCP谱及试剂盒抗体对其覆盖率情况。如果出现个别蛋白含量/丰度较高的情况,建议优化工艺或者采用定制化手段开发专属试剂盒。
Sample | Commercialized ELISA Kit | |||
DF | BackCalc.Conc. (ng/mL) | DF-corrected Conc. (ng/mL) | MRD (%) | |
20 | 85.5 | 1710.1 | / | |
40 | 50.3 | 2013.3 | 118% | |
80 | 32.2 | 2574 | 128% | |
160 | 19.7 | 3152.3 | 123% | |
Customized ELISA Kit | ||||
DF | BackCalc.Conc. (ng/mL) | DF-corrected Conc. (ng/mL) | MRD (%) | |
20 | 68.9 | 1377.3 | / | |
40 | 38.6 | 1543.6 | 112% | |
80 | 19.9 | 1592.8 | 103% | |
160 | 11.5 | 1834 | 115% | |
湖州申科基于客户实际样品的定制化开发实例。由于其实际样品中某一HCP占比较高(除总蛋白外),商业化试剂盒稀释线性适用不佳。通过抗体定制化服务,筛选符合要求的抗体组合,满足放行检测需求。
三、回收率异常:“真的是HCP吗?”
加标回收率偏离可接受范围(通常为70%-130%)是方法适用性失败的直接信号。其原因可能是由于基质干扰或是校准品与样品的HCP谱差异引起的。
• 精准纠正方案 1:稀释液筛选
商业化试剂盒的稀释液是广谱性的选择,但是对于特定产品可能并不适用,例如纯化中控样品、质粒、胰岛素等。在这种情况下,优先推荐在已验证样品基质MRD的情况下,采用样品基质作为稀释液进行测试。
Sample | Commercial Dilution Buffer | |||||
DF | BackCalc. (ng/mL) | DF-corrected. (ng/mL) | MRD (%) | Spike. (ng/mL) | Recovery (%) | |
32 | 138.6 | 4436.0 | / | 4 | / | |
64 | 56.4 | 3609.5 | 81% | 297% | ||
128 | 21.8 | 2785.0 | 77% | 287% | ||
256 | 7.9 | 2010.6 | 72% | 218% | ||
Customized Dilution Buffer | ||||||
DF | BackCalc. (ng/mL) | DF-corrected. (ng/mL) | MRD (%) | Spike. (ng/mL) | Recovery (%) | |
32 | 6.0 | 190.4 | / | 4 | / | |
64 | 3.0 | 193.7 | 102% | 86% | ||
128 | 1.2 | 159.0 | 82% | 90% | ||
256 | <LLOQ | <LLOQ | / | 90% | ||
湖州申科基于客户实际样品的稀释液筛选实例。在满足试剂盒性能情况下,对于回收率异常样品,优先建议以样品基质作为稀释液以快速解决方法学痛点。
• 精准纠正方案 2:抗原一致性评估与内部参比品的建立
在试剂盒早期选用时,应当评估实际样品HCP谱与目标试剂盒HCP校准品的匹配情况。如果差异过大,建议制备平台特异性HCP作为内部参比品。此参比品与实际样品HCP谱一致,可显著改善回收率偏差。

湖州申科提供基于客户实际样品的抗原一致性分析服务,有效规避方法开发风险。
结语:从"问题应对"到"质量源于设计"
HCP ELISA的技术挑战本质上是生物制品复杂性的镜像反映。与其被动应对异常数据,不如在工艺开发早期即引入多平台HCP分析策略:将ELISA作为高通量监测工具,辅以LC-MS/MS平台进行高风险HCP的鉴定与定量验证,建立“ELISA总HCP+MS特定HCP监控”的双平台体系。在监管日趋严格的背景下,只有深刻理解HCP ELISA方法局限性,并通过科学设计的实验方案和严谨的验证策略加以控制,才能确保HCP检测数据真正服务于产品质量与患者安全。
湖州申科提供针对HCP检测的全套解决方案和服务,涵盖高性能ELISA试剂盒、抗体开发服务、样品适用性验证、覆盖率验证、抗原一致性评估、高风险蛋白鉴定与定量及日常样品检测,旨在为生物制药客户提供从工艺开发到质量控制的全方位支持。我们的产品和服务不仅提供可靠的定量分析工具,还通过定制化服务和验证支持,帮助客户优化生产流程、降低风险并确保符合监管要求。