产品中心
在开发过程中,从校准品表征到抗体覆盖率,从供应稳定性到申报合规,每一步都可能成为“拦路虎”,湖州申科定制化平台帮您拨开检测迷雾,成为您HCP检测的“靠谱担当”。
USP<1132>章节内容中指出,基于ELISA方法原理的检测风险,定制化ELISA试剂盒的开发需要从以下方面进行评估:
• HCP校准品的工艺代表性,需充分表征;
• HCP校准品定量准确(赋值及量值可溯源);
• HCP多抗制备,覆盖率达到尽可能高的水平;
• 分析方法的良好检测性能:特异性、检测灵敏度、稀释线性等;
• 关键试剂供应制备量足够,满足产品生命周期。
为满足上述的开发要求,需要具备成熟的ELISA开发体系,强大的技术平台,专业的开发团队,稳健的生产平台,以实现稳定供应符合法规要求的定制化产品。
1. 完整的开发平台 保障产品性能
湖州申科在HCP ELISA检测技术领域深耕多年,已建立高质量的技术先进的HCP ELISA试剂盒全流程自有开发平台,涵盖抗原表征/制备、动物免疫、抗体制备、体系开发及验证平台,确保输出的HCP ELISA检测试剂盒性能满足用户申报需求。
2. 强大的技术能力 保障如期交付
在HCP开发技术的应用中,湖州申科自主研发了基于IMBS的抗体覆盖率检测方法和基于核酸文库的低丰度HCP富集技术,与权威机构合作完成多项课题且发表多篇学术成果。

同时,湖州申科已建立HCP分析表征最前沿的LC-MS技术平台,涵盖抗原一致性评价、覆盖率验证、生信分析、数据库等完整的HCP分析流程,以及低丰度HCP富集前处理专有技术,并开发了相关试剂盒;对于IMBS、LC-MS HCP检测技术按照方法验证要求进行了全面验证,满足法规要求,可用于申报,已服务国内外200+家生物医药企业。
3. 专业的开发团队 保障优质服务
开发团队成员硕博学历占比>80%,行业经验>5年,职责清晰,沟通无障碍,售后有保障。
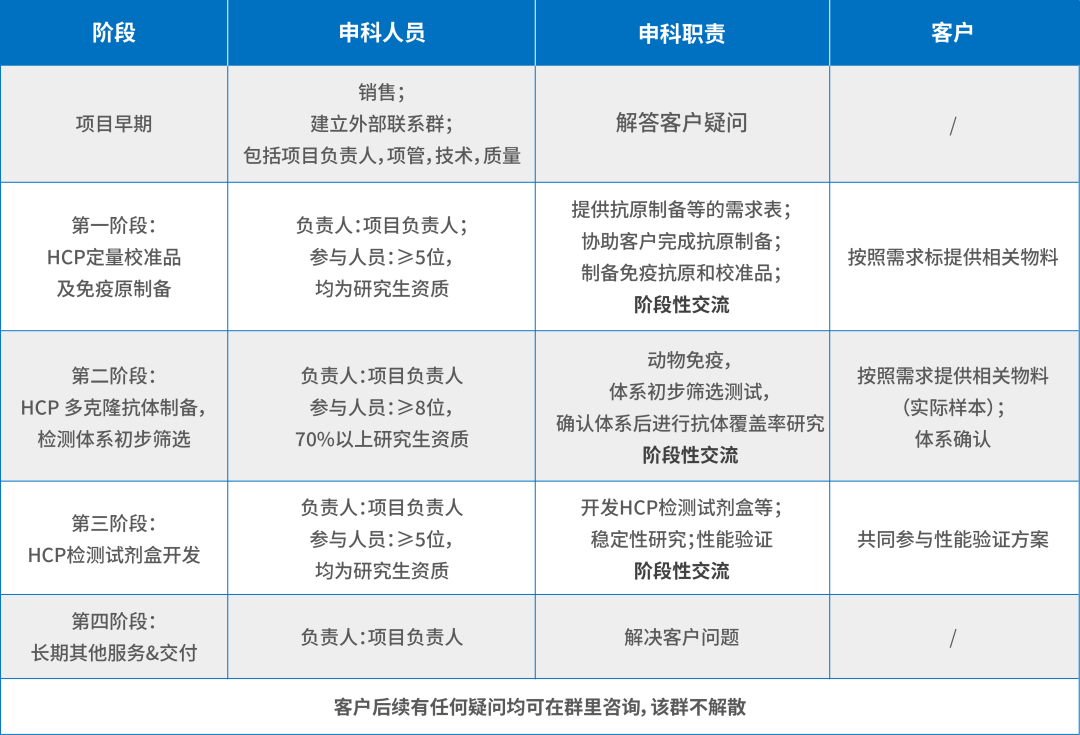
4. 自研自产,物料充足,保障稳定供应
• 校准品采用冻干形式大量制备,稳定保存10年以上;
• 抗体采用大动物免疫,其产量可生产≥10000盒,同批抗体满足10年以上供应;
• 试剂盒批内、披间具有良好的一致性。
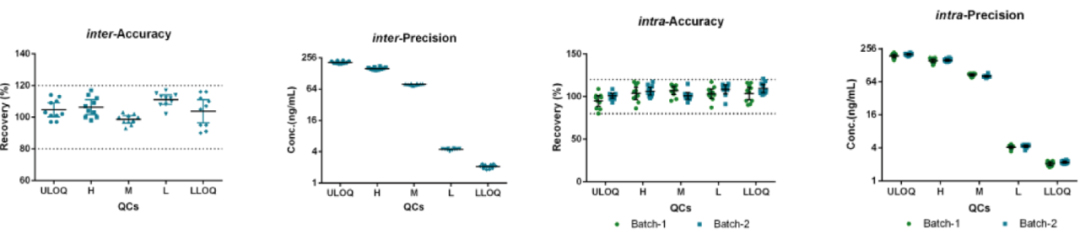
5. 符合法规要求,保障申报无忧
为确保客户使用开发的HCP ELISA检测产品符合申报要求,湖州申科的试剂盒定制化开发方案全流程严格按照法规要求,全过程符合CNAS质量保证体系,符合审计要求。
6. 众多用户的安心选择
湖州申科目前已承接常见宿主类型的HCP定制化开发,如期交付率达到100%,并成功协助客户实现中美、中欧申报。
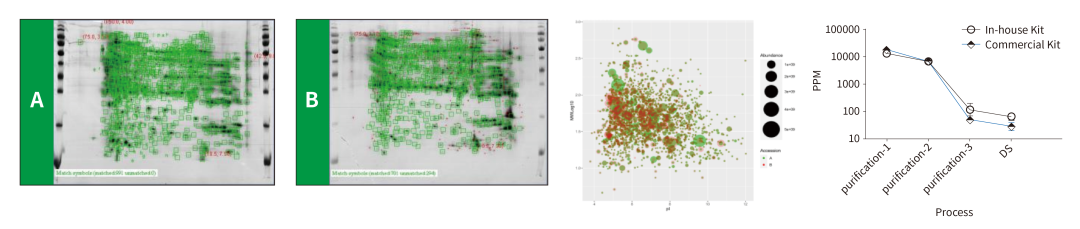
CHO HCP试剂盒定制化开发:基于IMBS-2D法,覆盖率≥75%;基于IMBS- LC/MS法,覆盖率≥90%;
开发的分析方法符合工艺流程HCP变化趋势。