产品中心
随着生物医药企业“出海”步伐的加快,除抗生素产品外,抗体药也成为了我国出海热门品类。全球药品监管要求持续提升,热原控制的合规要求迎来了关键升级!(点击链接了解更多→抗生素药品出海合规:关注非内毒素热原控制与MAT检测关键要求)
仅使用细菌内毒素检测法(BET,Bacterial Endotoxin Test)可能不足以完全评估控制热原风险,因此非内毒素热原(NEP,Non-Endotoxin Pyrogens)风险评估成为抗体药欧美药监的核心审查点。
一、MAT方法替代历程
(1) 欧洲药典(EP)法规要求
2025.07.01 起,EP 11.8 删除家兔热原法(RPT),MAT为唯一推荐替代方法;
EP12明确:仅用BET需提供NEP风险评估;MAT为可检测所有热原(含内毒素和NEP)的药典方法;
2026年起,EDQM核查将NEP控制策略列为高频缺陷项。
(2) 美国药典(USP)及相关标准
USP<1085>:经验证的等效的MAT法/ BET法,可替代家兔热原试验。
TRS 1043(单抗质量控制指南):仅用BET法时应进行NEP风险评估来确定进行致热原试验的必要性。而RPT重复性差、存在种属差异等,推荐MAT用于终产品热原放行检测。
USP替代性热原测试方法征集:2026年2月27日开始,全球征集非动物替代热原检测数据,重点评估 MAT,为USP-NF的潜在修订或新增通则提供信息。
二、NEP风险评估与控制
根据EP致热原性5.1.13章节要求:
为排除产品中存在NEP的可能性,建议在生产工艺开发阶段同时使用相同的3 批次进行BET和MAT交叉验证(若仅能提供1批次样品,则需对该批次开展3次独立试验以完成验证,且试验结果需满足可重复性精度要求)。
若生产工艺发生可能影响产品热原性的变更(例如使用不同原材料、变更生产场地或工艺参数),需重新进行风险评估。
对于所有拟用于肠胃外给药的产品,若无法排除NEP存在,则必须实施MAT试验。
2.6.30-6.5章节中关于NEP方法验证要求:
预实验应包括使用至少2种NEP配体(如肽聚糖、脂磷壁酸、合成细菌脂蛋白、鞭毛蛋白等)对检测系统进行验证,其中至少1种需加标至待检制剂中。
若有历史批次中已证实受NEP污染物污染的阳性样品,可优先使用;若没有,则可选择生产工艺可能引入的NEP对检测系统进行验证。
抗体药NEP发补描述实例:
关于家兔热原试验,应开展风险分析以评估产品中热原的潜在存在情况,并按照现行欧洲药典要求,采用体外方法进行热原检测。
如需获取抗体药NEP发补案例,可与我司联系。
三、抗体药工艺过程中NEP污染的关键诱因
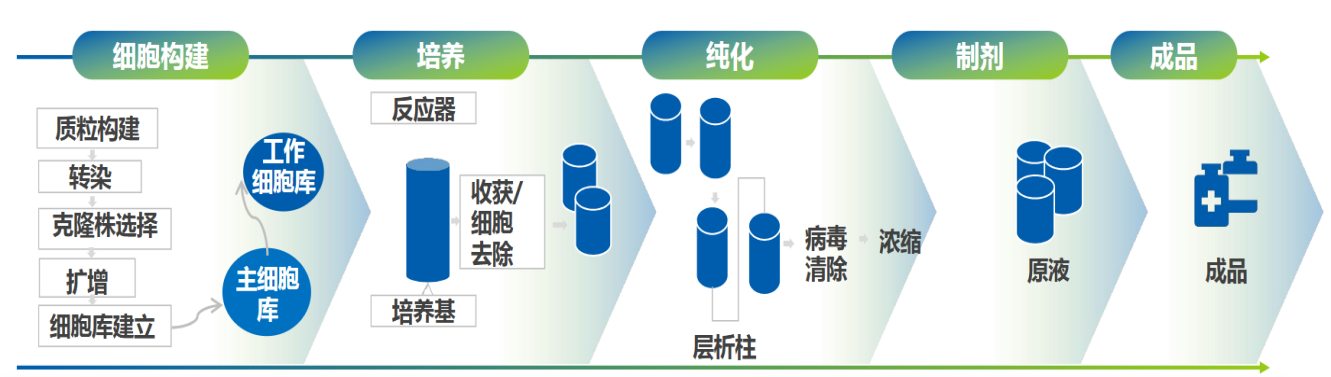
抗体药的开发生产涉及细胞株构建、细胞培养、蛋白纯化、制剂灌装等多个环节,NEP的产生与引入贯穿抗体药生产全流程,风险评估需覆盖所有可能导致致热性物质及相关影响因素。
以下为风险评估需考虑因素的非穷尽清单:
细胞培养:工程细胞的生长环境易滋生革兰氏阳性菌如脂磷壁酸(LTA)、肽聚糖等典型 NEP,且细胞自身代谢产生的宿主蛋白、内源性毒素也会成为NEP的来源。
纯化环节:层析填料、过滤耗材和缓冲液的去热原能力和残留,以及工艺操作中的交叉污染,可能会引入NEP。
其他:制剂制备的辅料、灌装环节的无菌环境管控不当,也可能会引入NEP。
这些NEP污染无法被BET识别,且易与微量内毒素协同作用,放大体内细胞因子分泌,引发严重的临床热原反应,成为抗体药临床应用的安全隐患。因此,欧美监管对抗体药NEP检测作出了硬性要求。
湖州申科以深厚基质分析能力为依托,针对样品特点提供精准解决方案,高效应对欧美注册申报和发补要求。在RPT替换MAT关键技术变更和NEP风险评估领域,提供从前处理开发到申报支持的全链条验证服务,切实降低合规风险,加速产品海外上市。
PyroSup™ 热原检测试剂盒(MAT法)核心优势:
合规性与申报基石:细胞来源清晰,获得保藏机构商业化授权,规避申报合规风险。
监管认可与性能稳定:联合权威机构进行全面性能验证,并经过客户及监管机构测试,其质量与性能得到保障和肯定。
完整的MAT解决方案:提供从方法开发、验证到申报资料撰写的全程技术支持。
成功案例:已成功支持多个产品完成欧盟/FDA上市申报,拥有成熟的项目经验。
资质认证:通过ISO13485质量管理体系认证和CNAS实验室认可,中、美、欧三地申报拥有丰富经验。
广泛样品适用性:覆盖抗体、疫苗、血液制品、医疗器械、化药、中药注射剂和原辅料等多种产品类型。
参考文献:
[1] Europaea, P. (2025) 2.6.30. Monocyte-activation test-11.8.
[2] Source: EDQM; Animal Welfare Progress; PA/PH/SG (07) 8
[3] 5.1.13. Pyrogenicity(EP12.3)
[4] 用于医药用途的单克隆抗体及相关产品的生产与质量控制指南(TRS 1043)