产品中心
在当今生物药行业高速发展的背景下,“多项目并行”已从一种运营策略演变为行业常态。
同一条生产线往往需要同时承载来自不同管线的多个单抗项目,每个项目背后都意味着独特的细胞株、差异化的原材料供应链、各异的工艺参数以及错综复杂的排期节奏。
这种高度集约化的生产模式虽然显著提升了产能利用率和资源周转效率,却也悄然将风险叠加至前所未有的水平——一旦某个项目在未加工收获液(UPB,Unprocessed Bulk)阶段发生外源因子污染,其影响绝不仅限于单一失败批次,更可能触发整条产线的连锁停摆,造成设备清场、验证重启、后续项目延期乃至客户信任危机,最终演变为一场系统性的交付灾难。
对于使用最广泛的工程细胞系CHO而言,UPB常见的外源因子污染有鼠细小病毒,Vesivirus 2117和支原体等。
• 鼠细小病毒(MVM):体积小、物理化学性质及其稳定,难以通过常规的过滤或灭活方法清除,是全球多起单抗生产污染事件的元凶。
• Vesivirus 2117 :在传统体外细胞培养法中容易漏检,极易在无预警情况下穿透整个生产流程。
• 支原体 :最小的自我复制原核微生物,缺乏细胞壁、生长缓慢且形态隐蔽。
因此,CHO细胞收获液对这些外源因子进行快速检测识别十分关键。
01 监管共识:风险识别,必须前移至UPB
全球监管机构早已明确释放信号:外源因子的风险控制必须前移至生产早期的未加工收获液关键节点。
○ICH Q5A (R2) 发布的《Viral Safety Evaluation of Biotechnology Products Derived From Cell Lines of Human or Animal OriginGuidance for Industry》强调UPB外源病毒检测是确保产品病毒安全性的三道互补防线中的关键一环,并明确要求对每一批UPB进行外源病毒检测。
○ FDA早在1997年发布的《Points to Consider in the Manufacture and Testing of Monoclonal Antibody Products for Human Use》强调对纯化工艺上游的UPB进行外源病毒和支原体检测,并且在检测中应侧重未过滤样品作为检测对象,同时如果检测出外源因子,则不得继续加工或使用该物料。
○ 2025年版《中国药典》亦在“人用重组单克隆抗体制品总论”中明确规定了每批次收获液要检测细菌内毒素及支原体等外源风险因子,应根据生产过程及所用材料的特点,在合适的阶段进行常规或特定的外源病毒污染检查。
这些法规动向共同指向一个核心逻辑:风险识别不能等到下游纯化完成才启动,而必须在UPB这一“临界点”完成确认。
同时监管机构正日益鼓励并接受采用先进技术替代耗时冗长的传统病毒检测方法。
ICH Q5A (R2) 指出基于对潜在污染物引入的风险评估,核酸检测(NAT)方法在未加工收获液阶段用于特定病毒(如鼠细小病毒)的检测,此类快速检测方法有助于实时决策。
表1. FDA指导文件对UPB、纯化中间品和成品的外源因子检测要求
检测项目 | UPB | 纯化中间品 | 成品 |
无菌性 (Sterility) | +* | + | + |
支原体 (Mycoplasma) | + | - | - |
外源病毒 (Adventitious Virus) | + | - | - |
种属特异性病毒 (Species-specific Virus) | + | - | - |
逆转录病毒 (Retrovirus) | + | - | - |
多核苷酸 (Polynucleotide) | - | + | - |
内毒素 (Endotoxin) | - | - | + |
02 传统检测耗时久,难匹配 GMP 生产节奏
支原体传统培养法需长达 28 天才能得出结果,外源病毒细胞培养法最快也需要 14 天,检测周期严重滞后于现代快节奏的 GMP 生产需求。若外源因子污染问题直到下游阶段,甚至成品放行前才被发现,企业将面临多重损失:
• 不得不面对高昂的处理成本;
• 原本紧密排布的多项目日程将因此全面紊乱,进而严重影响药品供应;
• 对于CDMO企业来讲,则严重损害客户对其交付能力的根本信心。
03 DetecInnova一体化检测平台:3 小时速检 UPB 外源因子
DetecInnova一体化检测平台基于NAT检测技术和独立微流控全自动分析系统,实现病毒/支原体自动提取、扩增、检测一体化操作。
该系统可在UPB阶段同步完成支原体和特异性病毒(MVM+VV-2117)的快速高灵敏度核酸检测,将关键结果确认时间压缩至3小时以内。加速 UPB 外源因子生物安全性检测时间。
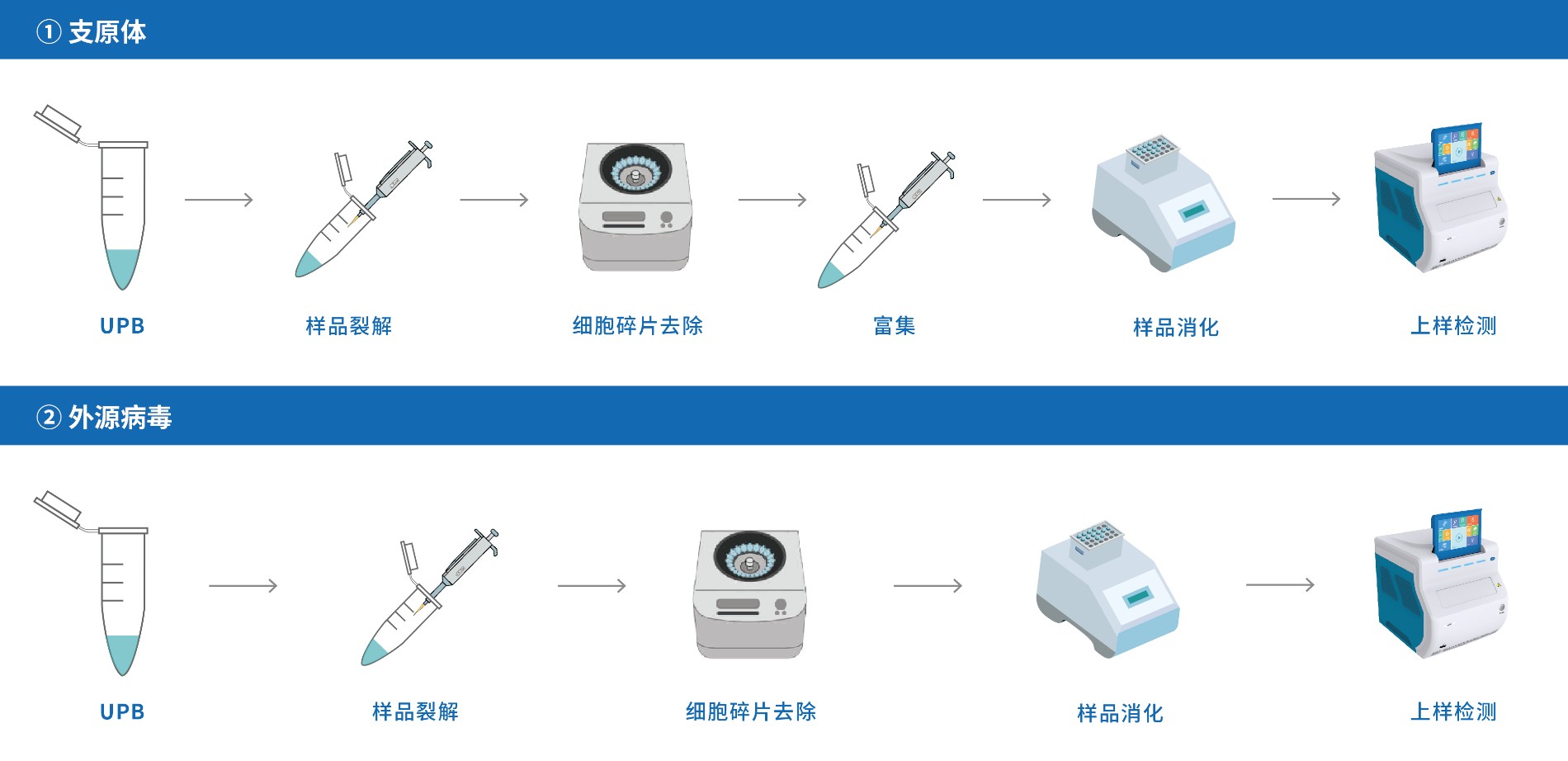
图1. UPB样品DetecInnova外源因子一体化检测流程
在抗体药物商业化生产的进程中,使用DetecInnova一体化检测平台符合当前使用NAT快速核酸检测方法的趋势,在物料正式进入昂贵且不可逆的下游纯化工序之前,帮助企业能够基于快速检测结果做出“放行”或“拦截”的决策。
04 风险前移:生物药企业高质量交付的核心战略
在多项目并行时代,真正成熟领先的企业必须具备“风险前移”的战略思维与技术落地能力,强化 GMP 风险控制形象,提升审计通过能力。
将病毒与支原体风险牢牢锁定在UPB阶段,不是简单增加一道检测工序,而是为整条高价值产线安装一道智能、敏捷、可靠的“最后一道安全阀”。这道安全阀的存在,让生产过程更加可预测,控制高价值批次损失,减少不确定库存占压。
对于多项目运行的CDMO企业,则可以让项目交付更加稳定可靠,也让客户在纷繁复杂的外包合作中获得真正的安心。
而这,正是未来生物药CDMO赢得长期信任与市场地位的关键所在。
DetecInnova一体化检测平台产品
货号 | 产品名称 | 规格 |
1603101 | 外源因子全自动核酸检测分析系统 (4 通道) | AdvSHENTEK-4system |
1603105 | 外源因子全自动核酸检测分析系统 (16 通道) | AdvSHENTEK-16system |
16031010411 | 一体化支原体检测卡 | 8 个 / 盒 |
16031010413 | 一体化CHO病毒(MVM/VV-2117)检测卡 | 8 个 / 盒 |