产品中心
 2023-12-07
2023-12-07
 0次浏览
0次浏览
病毒污染事件常见于使用工程细胞系表达的生物制品生产过程中。病毒污染可能来源于动物或人源细胞系本身,或来自细胞库建立时使用的动物源成分物料,例如牛血清和胰蛋白酶等。
因此生物药品制造商必须对原料,细胞库进行病毒安全风险分析,包括特定的牛源性病毒检测。以确保产品的安全性。
❖ 法规要求
《中国药典》规定,用于生物制品生产的细胞系需要进行检查是否有来源物种潜在的病毒,以及由于使用的原材料或操作带入的外源性病毒。其中若在生产者建库之前,细胞基质在建立或传代历史中使用了牛血清,则所建立的MCB或WCB和(或)生产终末细胞至少应按照通则 3604的要求检测一次牛源性病毒。
ICH,FDA,EMA等国外法规对细胞库检定的要求类似,ICH规定:对治疗用生物制品生产用细胞系和包括培养基在内的其它原料进行选择和检测,以确保其不含可能对人有感染和(或)致病作用的病毒;对生产工艺中清除感染性病毒的能力进行评估;在生产的适当步骤对产品进行测试,确保产品不存在感染性病毒的污染。
表1 《中国药典》对细胞检定项目中病毒检测要求
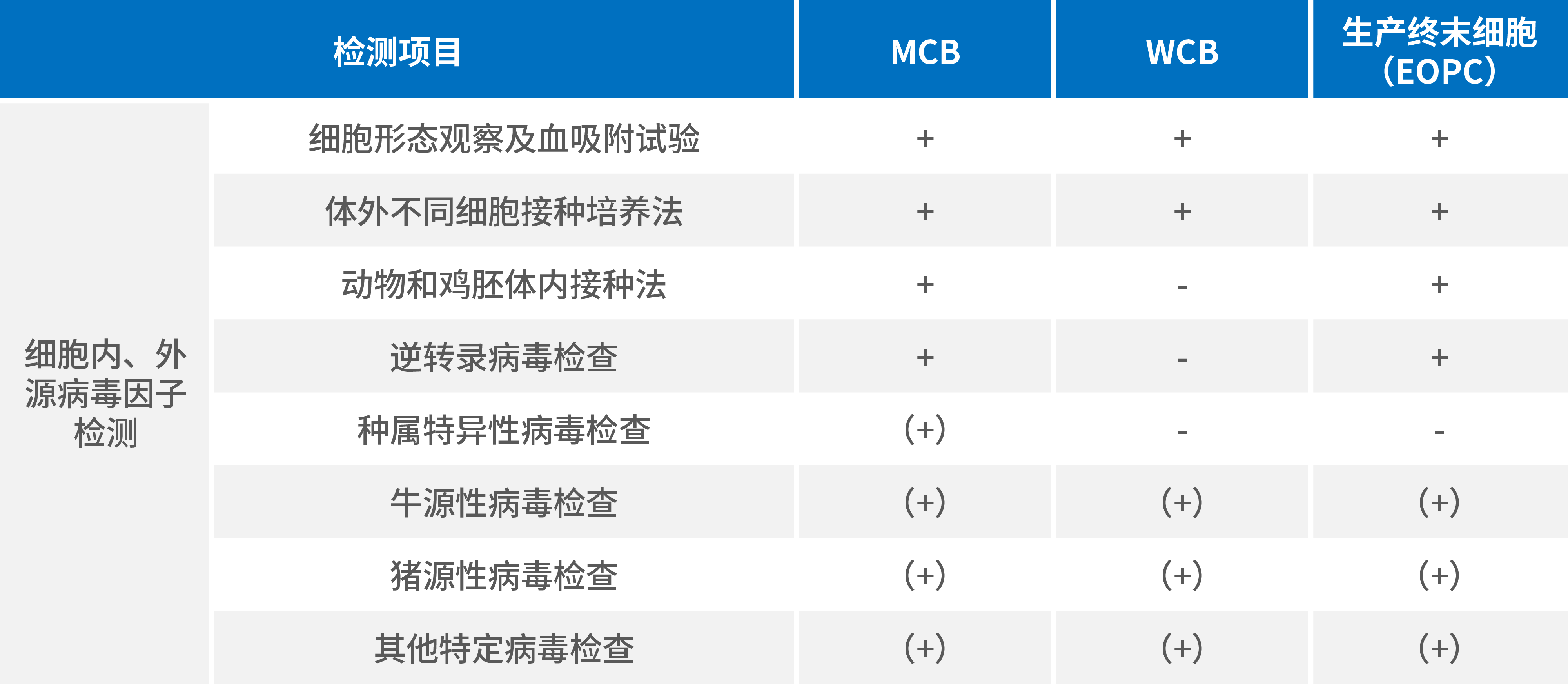
表2 ICH Q5A对细胞库病毒检测要求
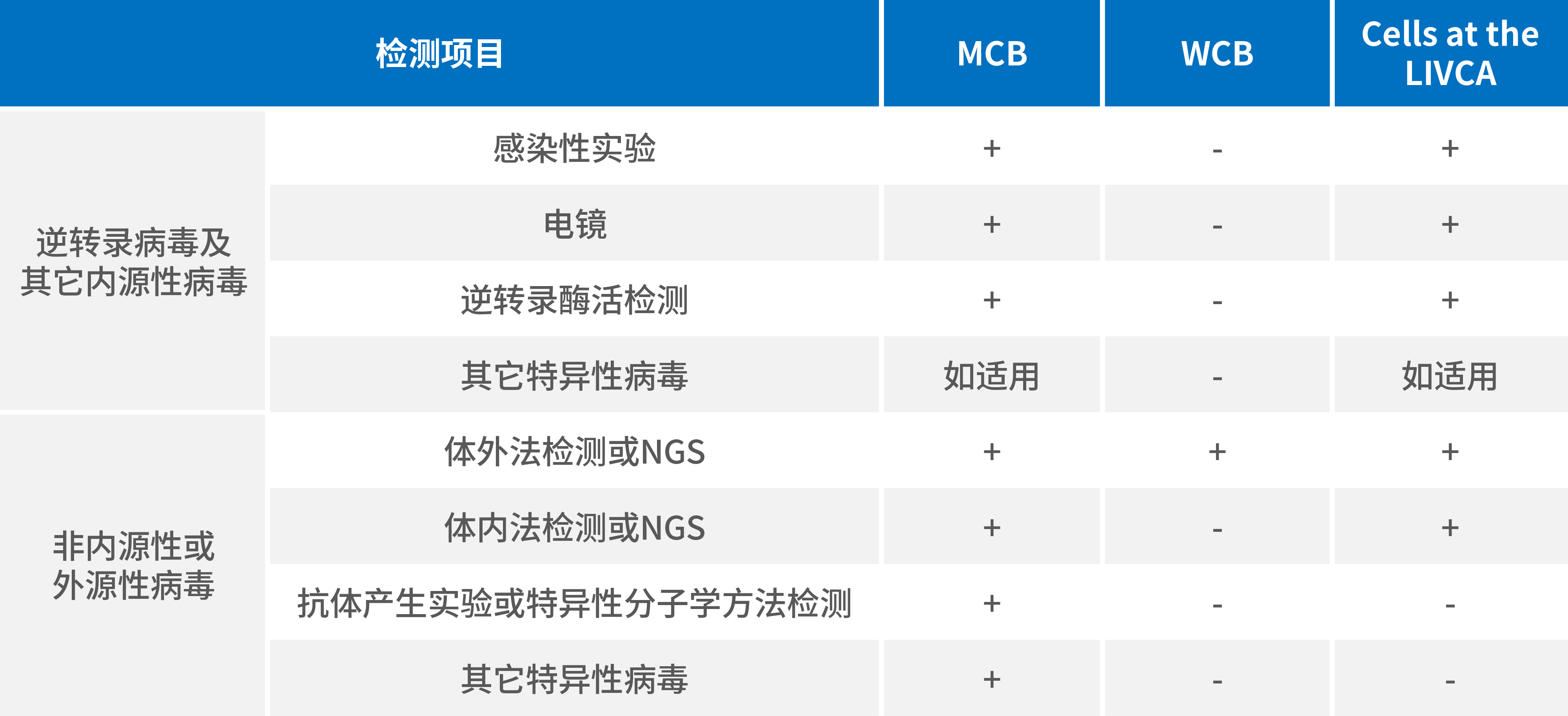
❖ 病毒检测方法
▪︎ 体外,体内检测方法:检测范围广,灵敏度高,检测条件要求高,耗时,费用高。
▪︎ 电镜(TEM):形态学观察,检测灵敏度有限。
▪︎ qPCR方法:高灵敏度的特异性病毒检测方法,耗时短,操作简便。
▪︎ NGS:检测范围广,灵敏度高,程序复杂。
传统的体外指示细胞法和体内动物接种实验具有实验周期长,通量低等局限性。根据ICH指南,基于细胞系的来源和传代历史,病毒特异性PCR或靶向分子生物学检测方法可用于补充或替代动物实验的方法。
湖州申科基于中国药典细胞库鉴定中对牛源病毒检测的要求,开发了牛源病毒(BVDV/REO-3/PI-3/BPV-3/BAV-3)多重核酸检测试剂盒(多重PCR-荧光探针法),试剂盒基于荧光探针的多重qPCR技术,实现在单孔内进行多靶标检测,灵敏度高,特异性强,稳定性好,经过全面性能验证,适用于牛血清和107细胞基质样品的病毒检测。
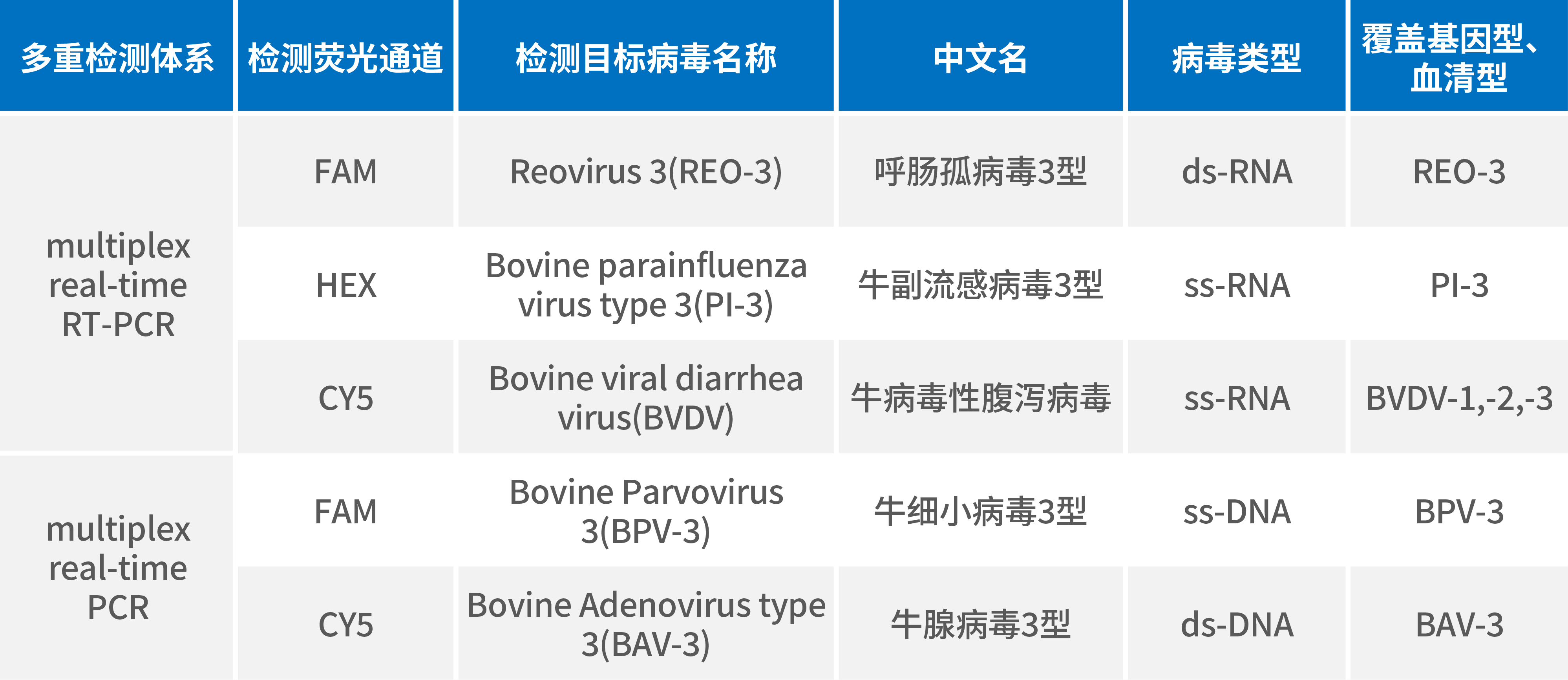
❖ 试剂盒性能
☑︎简便高效:基于多重PCR技术,一次检测多种病毒,效率高,节省时间人力。
☑︎灵敏度高:检测限达到10 copies/反应。
☑︎特异性强:多重检测通道互不干扰,与牛、猪基因组和CHO、Vero等8种常见工程细胞/菌均无交叉扩增。
☑︎结果可靠:检测包含内部质控IC,阳性对照PCS,阴性对照NCS,有效监控提取检测过程,避免假阳性,假阴性结果。
☑︎适用性:适用于10⁷细胞基质和牛血清复杂基质样本的检测。
使用SHENTEK®病毒核酸提取试剂盒(货号:1506730)和rHCDpurify®前处理系统可实现自动化、高效地从样品中回收病毒核酸。我们测试了从牛血清和10⁷ CHO-S细胞中提取检测DNA/RNA类型病毒,图1表明牛血清、细胞的病毒加标样品检测Ct值和纯病毒对照组的Ct值一致,说明该提取检测方法有效适用于牛血清和10⁷细胞基质样品类型。
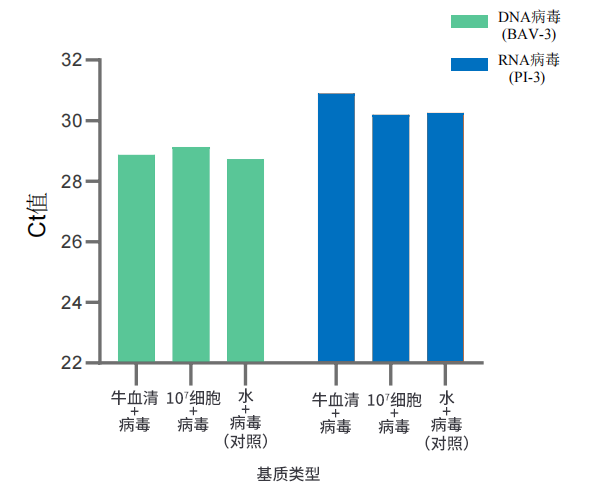
图1 SHENTEK®病毒核酸提取方法对于牛血清和10⁷细胞基质样品的检测效果
参考文献:
[2] ICH Q5A (R2) - Viral Safety Evaluation of Biotechnology Products Derived From Cell Lines of Human or Animal Origin
[3] 国家药典委员会及中国食品药品国际交流中心。治疗用生物制品病毒污染风险控制要点2021
[4] Characterization and Qualification of Cell Substrates and Other Biological Materials Used in the Production of Viral Vaccines for Infectious Disease Indications. FDA 2010
[5] 9 CFR 113.47 Detection of extraneous viruses by the fluorescent antibody technique.
[6] EMA 2013. Guideline on the use of bovine serum in the manufacture of human biological medicinal products