产品中心
 2022-11-08
2022-11-08
 0次浏览
0次浏览
中国仓鼠卵巢(CHO)细胞适合大规模工业培养,表达系统完善稳定,不易受到人类病毒感染,可表达人源糖基化修饰的优势,是生物制品制造中最常用的工程细胞。大多数的生物制剂以及几乎所有的抗体药物采用CHO表达生产。
中国药典规定,由CHO细胞表达生产的生物制品中相关宿主细胞蛋白残留量应不高于总蛋白含量的0.05%;美国药典规定的HCP水平限量值在1-100 ng/mg。
SHENTEK® CHO残留蛋白检测试剂盒(ELISA法),用于CHO细胞系表达的生物制品(单抗,重组蛋白,疫苗等) 中宿主细胞蛋白的残留检测。试剂盒按照法规要求进行了全面验证。特别是,试剂盒中的定量参考品、抗原及抗体覆盖率均采用2D和LC-MS两种方法进行了表征和验证,严格遵循ISO13485质量体系,各项性能满足CHO HCP检测需求。
● 货号:1301304 CHO HCP检测试剂盒(酶联免疫吸附法) ● 货号:1303382 抗CHO-HCP抗体(绵羊)
● 货号:1303383 阴性抗体(绵羊) ● 货号:1301307 CHO HCP质控品
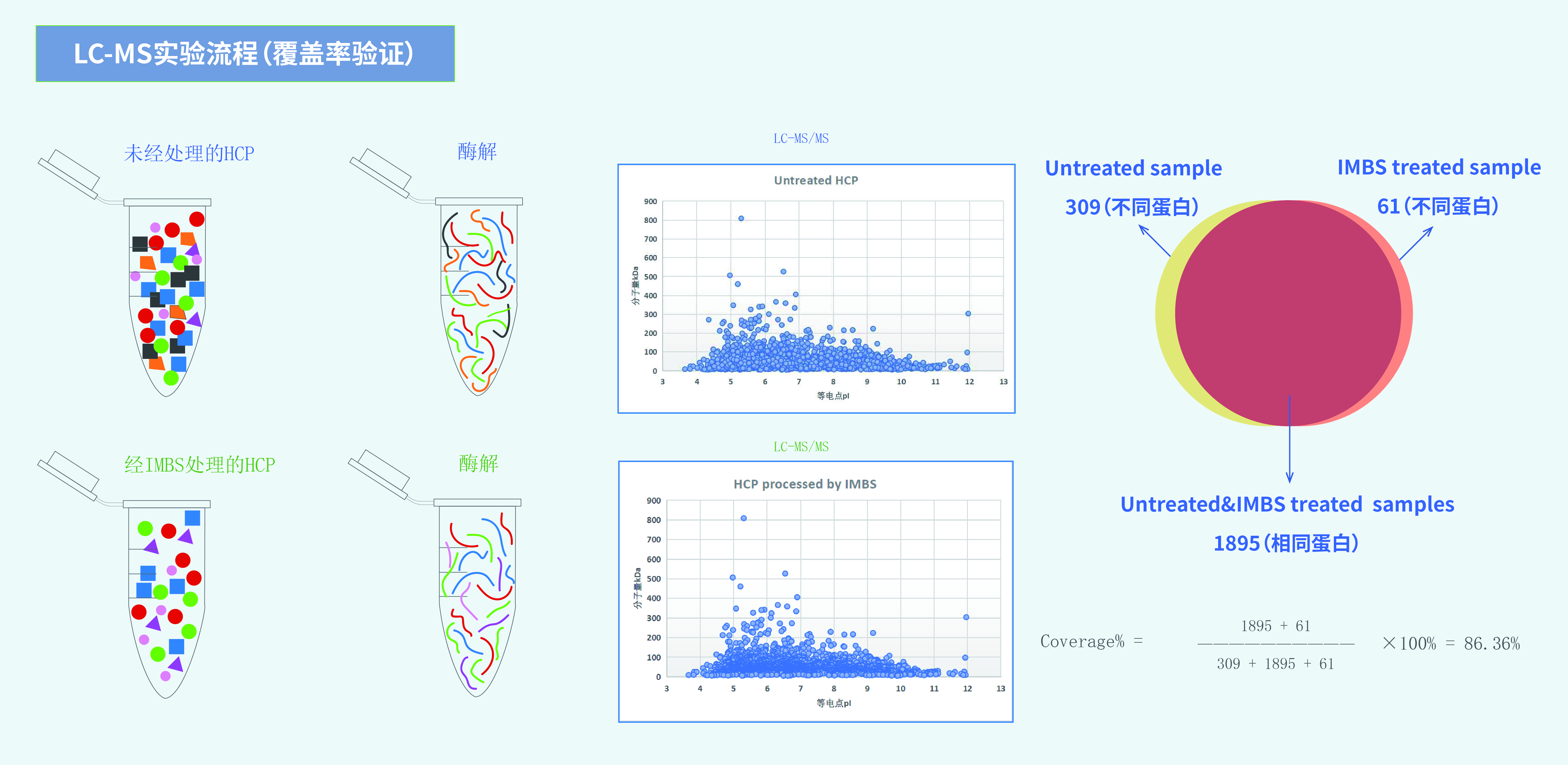
图1 CHO-HCP 抗体覆盖率(>85%)验证
采用IMBS&LC-MS方法检测,可检测到CHO HCP 2000多个,其中包含了有文献报告的CHO HCPs中的相关高风险蛋白。
▋ 技术参数
技术原理:ELISA双抗体夹心法;
线性范围:1-128ng/mL,相关系数R²>0.990;
定量限:1.5 ng/mL;
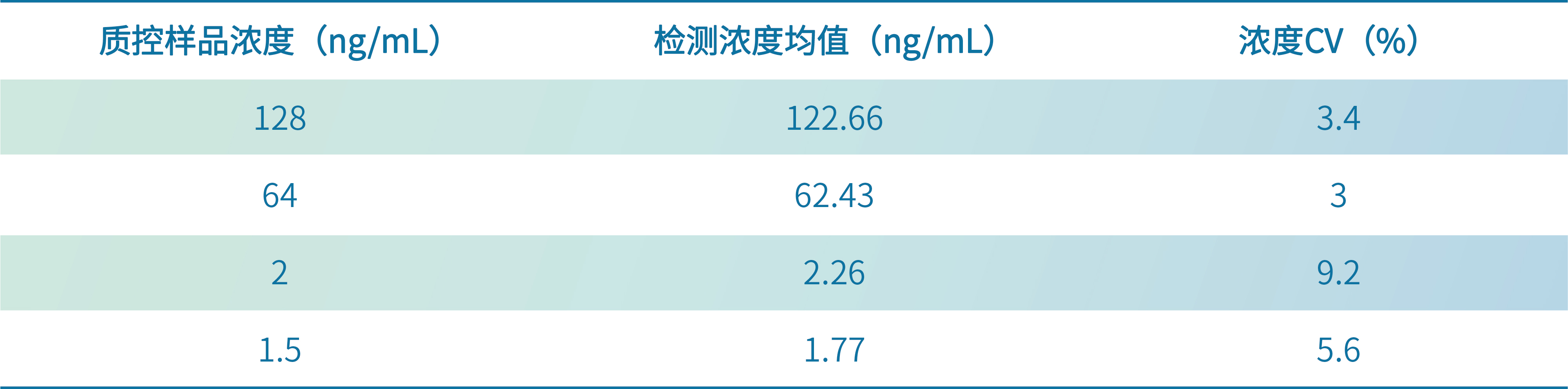
重复性:CV<15%,定量限浓度CV≤20%;
准确度:回收率范围80%~120%,CV≤20%;
特异性:与Vero、HEK293T、汉逊酵母和E.coli等宿主蛋白无交叉反应;
适用性:实验验证多种样本基质,且样品稀释后的HCP呈线性;
覆盖率:
◆ 风险因子:校准品和HCP抗体均能覆盖CHO HCP常见高风险因子;
◆ 方法验证:采用IMBS-2D和IMBS-MS两种方法正交检测抗体覆盖率;
稳定性:批内和批间一致性高,结果稳定。
表1 每个浓度样品20孔复测的准确性和重复性
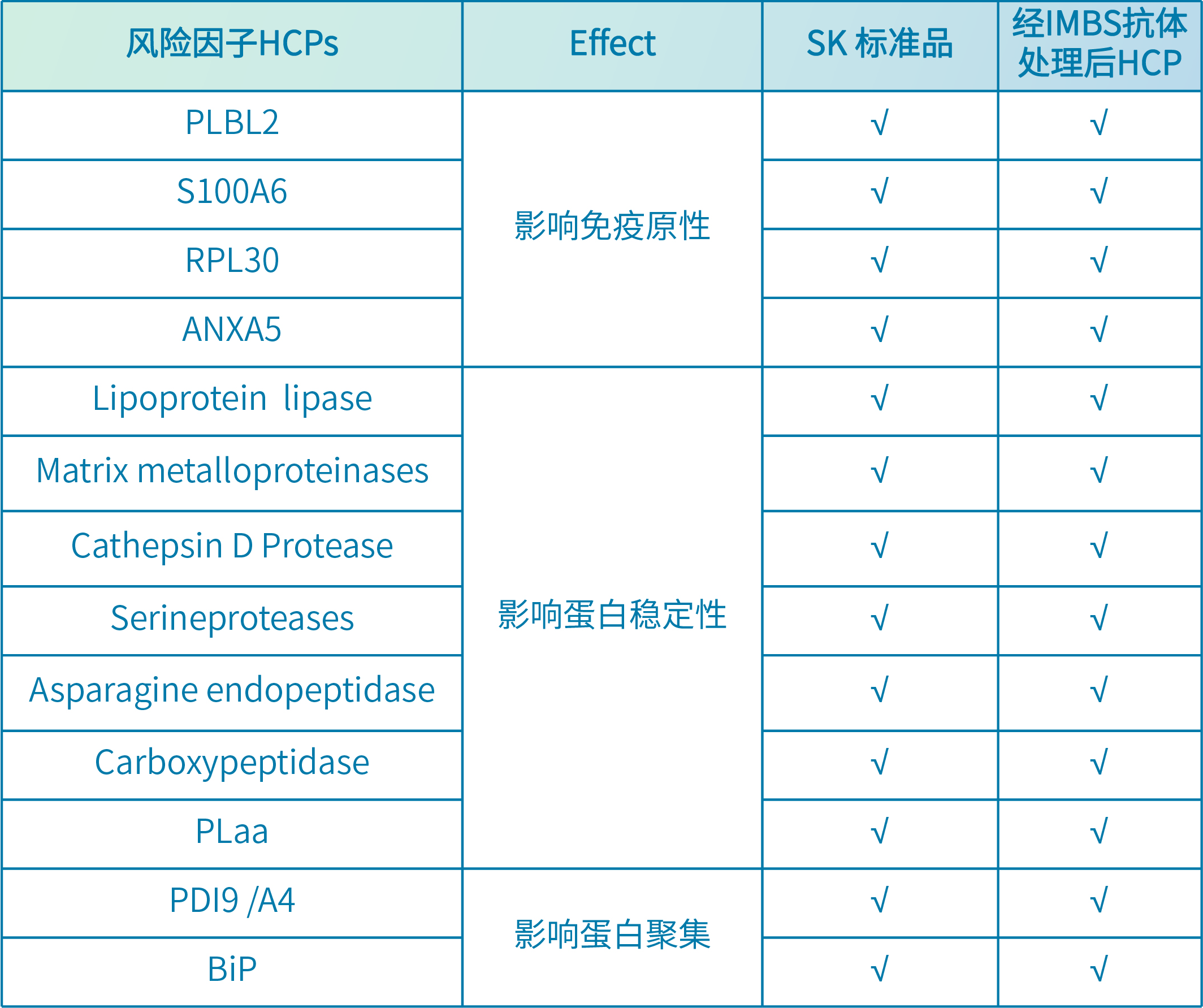
▋ 高风险CHO HCPs
HCPs危害程度与HCPs本身的特性功能有关,需要识别特定的HCPs对药品质量和病患安全的影响:
❶ 高免疫原性,可能诱发人体不良免疫反应;
❷ 类免疫佐剂作用,激发人体对药品本身免疫反应,降低药效;
❸ 含有生物活性物质,可能导致药效变化;
❹ 潜在的蛋白酶或“吐温酶”活性,可能导致产品稳定性下降,药效变化;
通过LC-MS方法对校准品和IMBS抗体处理后的CHO HCPs分析,均可检测到高风险HCPs。