支原体检测(传统法+qPCR法)
在生物制药与细胞治疗生产过程中,支原体污染是影响产品安全性的关键质量属性。支原体是一类无细胞壁、可通过0.2 μm滤膜的最小的原核细胞型微生物,在细胞培养中难以被察觉——它通常不引起培养液浑浊,在标准光学显微镜下不可见,却能严重影响细胞的表型特征和正常生长,给药品质量安全控制带来极大的风险。
• 《中国药典》2025版3301规定:主细胞库、工作细胞库、病毒种子批、对照细胞及临床治疗用细胞进行支原体检查时,应同时采用培养法和指示细胞培养法(DNA染色法),也可采用经国家药品检定机构认可的其他方法(如qPCR法)。
• 美国药典(USP)、欧洲药典(EP 2.6.7)及日本药典(JP)等也均要求对原材料、细胞库、病毒种子批、未加工收获液及终产品进行支原体控制。
目前支原体检测主要由三种方法:
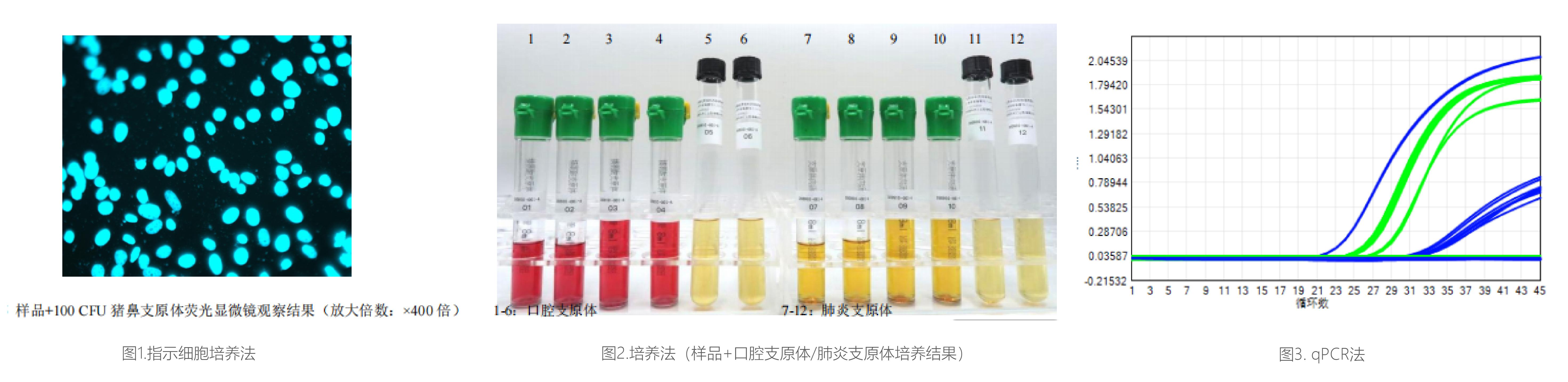
• 培养法:将供试品接种于特定培养基中,在适宜环境下培养28天,通过观察培养基变化及支原体特征性状菌落进行判定。该方法是药典规定的“金标准”之一,但检测周期长,且需阳性活菌作对照,对实验室环境要求较高。
• 指示细胞培养法(DNA染色法):将供试品接种于指示细胞(无污染的Vero细胞或经国家药品检定机构认可的其他细胞)中培养后,用DNA特异性荧光染料染色,在荧光显微镜下观察支原体DNA着色情况——支原体污染的细胞表面及周围会出现特征性的荧光着色颗粒。该方法对难以培养的支原体菌株尤为有效。
• qPCR法(核酸扩增技术):针对支原体16S rRNA等保守序列设计引物探针,采用TaqMan荧光探针法定量检测样本中的支原体DNA。该方法全程仅需几小时,灵敏度高(可达10 CFU/mL) ,可覆盖多个种属支原体。EP 2.6.7、USP <63>及JP均已正式收录NAT方法,其替代传统方法的前提是完成充分的验证——检测限达到10 CFU/mL可替代培养法,达到100 CFU/mL可替代指示细胞培养法。
支原体检测方法的选择是科学性、法规性与风险管控的综合平衡,建议遵循药典优先、方法互补两大核心原则,以实现检测方法的风险适配与阶段匹配。
• 药典优先:培养法与指示细胞培养法为各国药典明确的金标准方法,主要用于主细胞库、工作细胞库、病毒种子批及终产品的合规放行与最终结论判定,结果具备最高法规效力;
• 方法互补:qPCR 快速检测法则凭借检测速度快、灵敏度高、通量高、操作便捷的优势,在原材料入厂筛查、生产过程监控、细胞治疗产品紧急放行等场景中发挥不可替代的作用。
将金标准方法与快速方法科学组合、分层应用,可构建覆盖生物制品研发、生产、放行全生命周期的支原体污染防控与质量保障体系。
湖州申科聚焦生物安全质控需求,提供覆盖传统药典方法与 qPCR 快速方法的全链条检测解决方案,助力企业实现合规、高效、稳定的支原体管控。
• 平台资质:ISO13485:2016认证;CNAS认可;BSL-2加强型实验室;
• 数据可靠:符合《中国药品检验标准操作规范》、《药品检验仪器操作规程》及21 CFR Part 11电子记录管理要求;
• 合规的检测体系:MycoSHENTEK®支原体检测试剂盒(2G)经三方室间验证,灵敏度可达10 CFU/mL,覆盖支原体及相关菌属约200种;现已获得FDA DMF备案 (MF29624);
• 高质量菌株保障:MycoSHENTEK®支原体验证菌株获正式授权,溯源至知名保藏机构;参照EP2.6.7关于G/C比的要求,于指数生长期收获,确保菌株参考品的高活力。
| 方法 | 样品要求 | 项目周期 |
| 培养法 | 6mL样品 | 35个工作日 |
指示细胞培养法 | 2mL样品 | 35个工作日 |
qPCR法 | 2mL样品 | 10个工作 |