产品中心
 2022-06-02
2022-06-02
 0次浏览
0次浏览
支原体是一种无细胞壁的已知体积最小的原核微生物,其大小介于细菌和病毒之间(直径约0.1-0.8 µm),因此一般细菌过滤器(0.22 µm)无法有效去除。支原体污染在细胞培养领域普遍存在。
支原体污染风险
支原体严重影响培养中的细胞的表型特征和正常生长,给药品质量安全控制带来了极大的风险。因此,细胞培养过程中的支原体检测非常必要。与细菌、真菌污染不同的是,支原体的存在不一定导致培养液浑浊或细胞的可见改变,因此需要合适的方法进行检测。
FDA、WHO等不同国家和地区监管机构和USP、EP、ChP等法规均对支原体检查提出了要求,主要包括测试细胞库(主细胞库、工作细胞库),收获前的下游细胞培养物,终产品以及对照细胞等是否受到支原体污染。
▋ 支原体核酸法的法规要求:
传统的检测方法主要有培养法和指示细胞法,一般要求同时进行检测。这2种方法通常需要较长时间,如培养法至少28天。近年来,细胞治疗药物快速发展,且其上市周期快,货架期短,培养法和指示细胞法均无法满足药物放行的时间要求。
核酸扩增技术(NAT),如荧光探针qPCR检测方法由于其检测时间短和特异性好等优势而被用于支原体检测。作为替代方法,NAT检测方法需确证能达到法规所要求的检测灵敏度。检测灵敏度达到10CFU/mL,可替代培养法;达到 100CFU/mL,可替代指示细胞培养法。
合适的支原体标准菌株是进行支原体NAT检测方法验证的首要条件。基于污染的发生频率和进化关系,中国、欧洲、美国、日本4个国家和地区的药典一致提出优先使用猪鼻支原体、口腔支原体、肺炎支原体3种支原体作为标准菌株进行NAT方法检测限的验证。
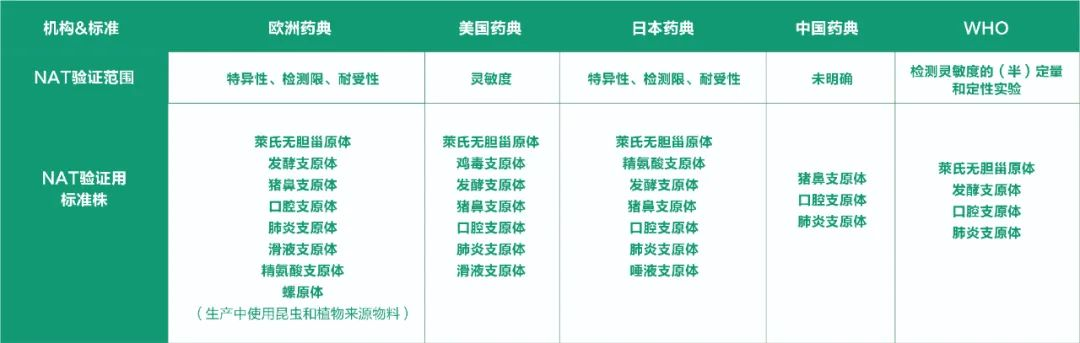
不同国家监管机构和法规对支原体NAT检测的认可及验证要求
▋ 支原体NAT法验证要求总结
检测限:
● 检测限的界定要求必须针对每种支原体确定阳性检测临界值。
● 每种支原体必须至少进行三次独立的10倍梯度稀释液检测,且每次检测中每种稀释液浓度都必须制备平行管进行检测,以使各稀释液浓度的检测结果达到24个。
● 阳性临界值指的是至少能够使95%的试验运行检测得到阳性结果的支原体浓度,即24个样品(4x6或3x8)中至少要取得23个有效的阳性检测结果。
特异性:
● NAT检测的挑战是要使用针对多种支原体都具有适用性的PCR引物。体系覆盖的检测种类越多,其特异性可能会受到影响。例如,革兰氏阳性菌与支原体具有密切的系统进化相关性,PCR可能会检测到这种细菌属,从而产生交叉检测的结果。
稳健性:
● 需要证实NAT检测法是否能够在方法参数发生人为引起的微小变化时结果不受影响。
可比性:
可比性的评估应包含NAT检测法与药典检测法的LOD对比。规定了以下要求:
● 以NAT法代替培养法:需要证实检测限达到≤10CFU/ml;
● 用NAT法代替指示细胞培养法:对每种被测支原体的检测限都必须达到≤10CFU/ml;
● 在这两种情况下,采用NAT法的检测和采用传统方法的检测必须同时进行,以使用相同样本(CFU可比性)对它们的LOD进行同步评估。
MycoSHENTEK®支原体检标准品
湖州申科提供两类支原体标准品:支原体验证菌株和支原体DNA校准品,可用于NAT方法的适用性验证。
▋ 支原体验证菌株
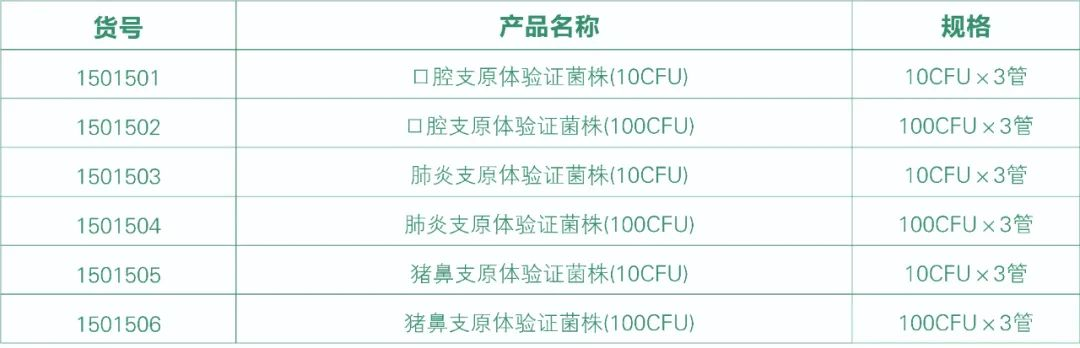
湖州申科现提供口腔、肺炎、猪鼻支原体3种支原体验证用标准菌株,溯源至知名保藏机构,获得正式授权。后续将推出其他验证用标准株。标准菌株标定至10CFU和100CFU浓度,经培养法和dPCR方法检测,满足支原体检测方法验证用需求。
MycoSHENTEK®支原体验证菌株为灭活的支原体菌液,无感染风险;经培养法测定CFU (Colony Forming Units),dPCR法测定GC (Genomic Copies),定量测定,质量可控;每管含10CFU或100CFU支原体,加入相应体积的样品基质中即可用于验证。
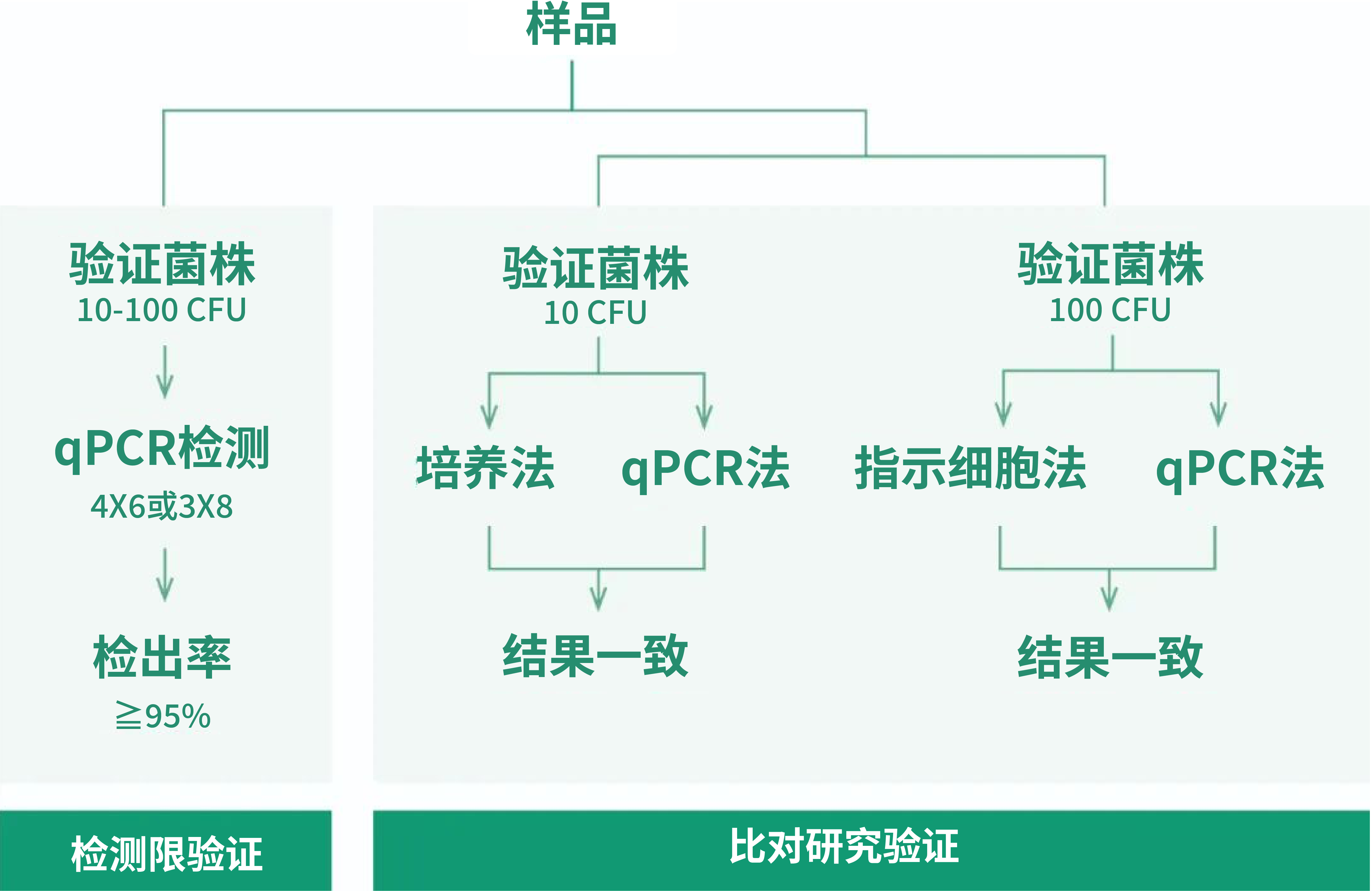
▼ 标准菌株检测限验证流程
▋ 支原体DNA校准品
MycoSHENTEK®支原体DNA校准品为质粒DNA,无感染风险,可用作定量标准品;采用DNA 稀释液进行系列梯度稀释,可用于验证检测灵敏度和校准品浓度对数与Ct值的线性关系,操作方便;不受其他种属DNA干扰,专属性强,耐用性高。

MycoSHENTEK®支原体提取和检测试剂盒,可用于提取纯化样品中微量支原体DNA并定性检测主细胞库、工作细胞库、病毒种子批以及临床治疗用细胞中是否有支原体污染。
提取纯化试剂盒采用磁珠法,回收率高,样品兼容性好,配合rHCDpurify®前处理系统,实现自动化提取操作。检测试剂盒采用荧光探针技术(qPCR法),覆盖120多种支原体DNA序列,检测快速,专一性强,不同品牌PCR仪器适用性表现良好,性能可靠。

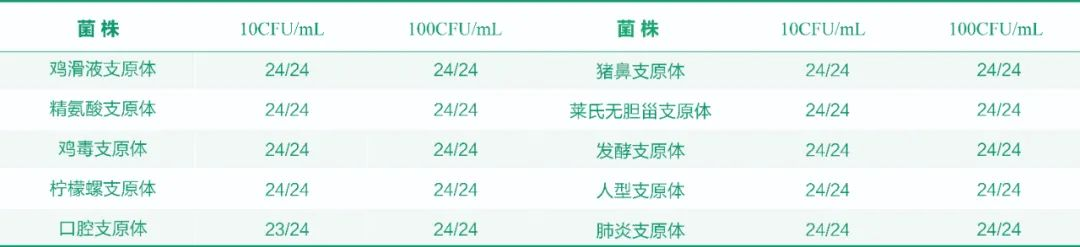
支原体检出率-阳性数/总数
MycoSHENTEK®支原体DNA检测试剂盒参照 EP 2.6.7 和 JP XVII 支原体检测相关要求进行了全面性能验证,符合对支原体验证的所有要求,灵敏度高(达到10CFU/mL),可替代培养法和指示细胞培养法,是目前国内首个经过三方室间验证的,性能完全符合药典要求的支原体检测试剂盒。